Galvenā atšķirība: molaritāte, kas pazīstama arī kā molārā koncentrācija, mēra vielas daudzumu molu daudzumu litrā šķīduma. Molaritāte ir apzīmēta ar kapitālu. M. Molality mēra vielas daudzumu, kas ir vielas šķīdinātāja kilogramā. Molalitāte ir apzīmēta ar mazāku burtu m.
Abi jēdzieni pamato savus aprēķinus par to, cik molu ir pašreizējā risinājumā. Šķīdumu var definēt kā homogēnu maisījumu, kas nozīmē, ka divas vai vairākas sastāvdaļas ir sajauktas līdz vietai, ka to nevar atšķirt ar neapbruņotu aci. Šie divi jēdzieni prasa izpratni par molu, jo tas nosaka šķīdumā esošo molu skaitu. Molu teoriju atklāja itāļu zinātnieks Amedeo Avogardo.
1811. gadā Avogardo ierosināja, ka gāzes daudzums noteiktā temperatūrā un spiedienā ir proporcionāls atomu vai molekulu skaitam neatkarīgi no tā veida. Šī koncepcija ir pazīstama kā Avogardo konstante. To definē kā sastāvdaļu (parasti atomu vai molekulu) skaitu vienā noteiktā vielas molā. Vienkāršā izteiksmē viens mols vielas pārstāvētu elementos esošo atomu un molekulu skaitu. Piemēram: Skābekļa atomu svars ir 16, tas būtu skābekļa masas masa. Tātad, viena mola skābekļa masa būtu 16 grami. Saskaņā ar Avogardo, vienam mola skābeklim būtu tāds pats atomu skaits kā vienam molam ūdeņraža. Tomēr tie var atšķirties pēc svara.
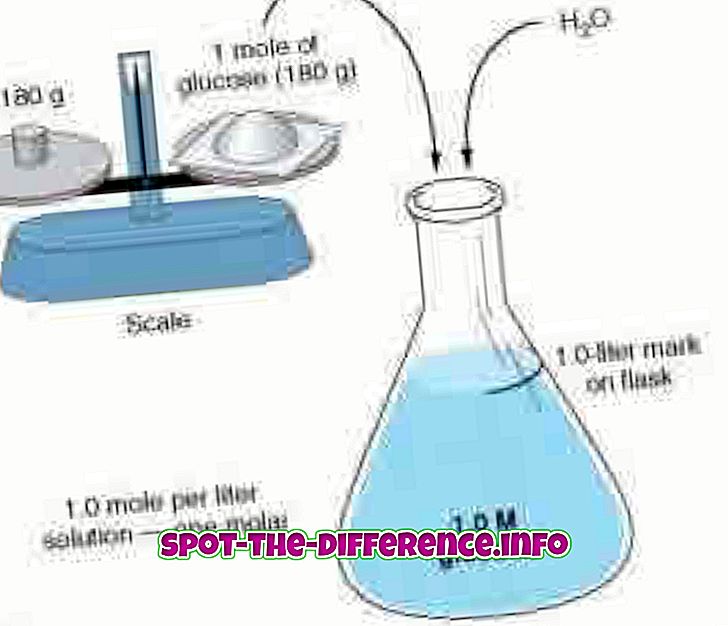
Molaritāte un molalitāte mēra koncentrāciju, izmantojot divas atšķirīgas pieejas. Molaritāte, kas pazīstama arī kā molārā koncentrācija, mēra vielas daudzumu molu daudzumu litrā šķīduma. Molaritāte ir apzīmēta ar kapitālu M. Tātad risinājums ar 1, 0M norāda, ka tas satur 1 molu šķīduma uz litru šķīduma. Piemēram: ūdens un cukura šķīdums. Ja šķīdumu mēra kā 1, 0 M, tad šķīdumam ir 1 mols cukura uz vienu litru šķīduma. Molaritāte ir pazīstama arī kā vielas koncentrācija, koncentrācija, vielas koncentrācija vai vienkārši koncentrācija. Molaritāti var aprēķināt, izmantojot formulu: M = mol (molu daudzums) / L (šķīduma tilpums litros).

Molalitāte mēra vielas daudzumu molu daudzumu uz kilogramu šķīdinātāja. Molalitāte ir apzīmēta ar mazāku burtu m. Tātad risinājums ar 1, 0 m norāda, ka tas satur 1 molu šķīdinātāja uz kilogramu šķīdinātāja. Atšķirīsim šķīdinātāju no šķīdinātāja. Šķīdinātājs ir viela, kas tiek izšķīdināta citā vielā. Šķīdinātājs ir viela, kas izšķīdina šķīdinātāju. Tātad, ja ūdeni un cukuru sajauc kopā, cukurs būtu šķīdinātājs un izšķīdina šķīdinātāju. Šķīdums būtu jauktais cukura ūdens. Tagad, molalitātes ziņā, ir ārkārtīgi svarīgi, lai molu dalītu ar šķīdinātāja masu, nevis šķīdumu. Molalitāti var aprēķināt, izmantojot formulu: m = mol (molu daudzums) / KG (šķīdinātāja masa kg).
Kāpēc atšķirība? Nu, abi tiek izmantoti, risinot temperatūru. Ja risinājums mainīs temperatūru, tiek izmantota molalitāte. Bet risinājumiem, kas paliks nemainīgā temperatūrā, tiek izmantota molaritāte. Tas ir tāpēc, ka, paaugstinoties vai nokritoties temperatūrai, šķīduma apjoms mainās un tas tieši ietekmē molaritāti. Tādējādi koncentrācijas aprēķināšanai tiek izmantota molalitāte.