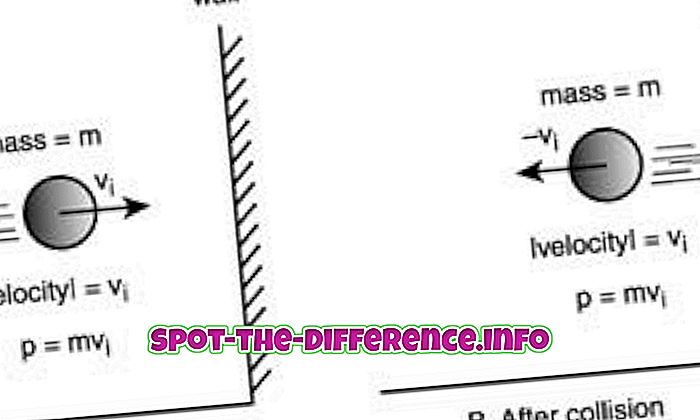
Galvenā atšķirība: oksidēšana un reducēšana ir divi procesi, kas notiek redoksreakcijā. Oksidācijā molekula, atoms vai jonu oksidācijas stāvoklis palielinās vai būtībā tas zaudē elektronus. Samazināšanā molekula, atoms vai jonu oksidācijas stāvoklis samazinās vai drīzāk tas iegūst elektronus.

Oksidācijā molekula, atoms vai jonu oksidācijas stāvoklis palielinās vai būtībā tas zaudē elektronus. Samazinājums būtībā ir pretējs tam. Samazināšanā molekula, atoms vai jonu oksidācijas stāvoklis samazinās vai drīzāk tas iegūst elektronus.
Oksidēšana un samazināšana vienmēr notiek vienlaicīgi. Tas ir galvenokārt tāpēc, ka molekula, atoms vai jonu zaudē elektronu; elektronam jāiet kaut kur; ti, uz citu molekulu, atomu vai jonu. Šī molekula, atoms vai jonu savukārt iegūst zaudēto elektronu.
Apskatīsim piemēru:
H 2 + F 2 → 2 HF
Sadalīsim tos uz atomiem un joniem:
H 2 → 2 H + + 2 e−
Ūdeņraža molekula zaudē divus elektronus, lai kļūtu par diviem ūdeņraža joniem. Būtībā tā ir oksidācijas reakcija, jo tā ietvēra elektronu zudumu.
F 2 + 2 e− → 2 F−
Fluors iegūst divus ūdeņraža molekulas zaudētos elektronus, lai kļūtu par diviem fluora joniem. Tas būtībā ir samazinājuma reakcija, jo tā ietvēra elektronu pieaugumu.
2 H + + 2 F− → 2 HF

Tādējādi visas redox reakcijas var rakstīt kā:
H 2 + F 2 → 2 HF
Kaut arī oksidēšanās un reducēšanās notiek molekulā vai atoma līmenī, mūsu ikdienas dzīvē joprojām ir iespēja redzēt redoksreakcijas. Daži redoksreakcijas piemēri ir dzelzs rūsēšana; ābolu brūna; balinātāju plankumu sadalīšana utt.